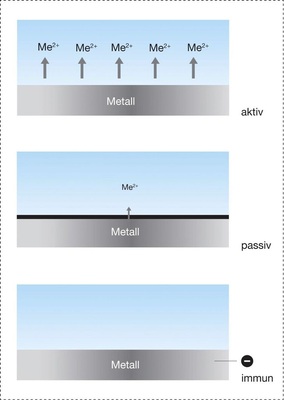
Für ein Metall in seiner wässrigen Umgebung gibt es drei mögliche Zustände. Erstens: Das Metall (z.B. Eisen) verhält sich aktiv und geht in Lösung, wie man das von der Rostwasserbildung her kennt. Zweitens: Auf dem Metall bildet sich eine Deckschicht aus, die dicht und fest haftend die Oberfläche verschließt. Dabei geht nur sehr wenig Metall ins Wasser über, der Korrosionsprozess kommt praktisch zum Stillstand. Erreicht wird das bei Eisen nur bei entsprechend hohen pH-Werten. Im dritten Fall verhält sich das Metall in seiner wässrigen Umgebung immun, es korrodiert nicht. Möglich wird dies durch Anlegen einer negativen (Schutz-)Spannung, wie man das vom kathodischen Boilerschutz z.B. auch mithilfe von Magnesiumopferelektroden her kennt.
Entsalzung bremst die Sauerstoff- und Lochkorrosion
Fehlen die gelösten Salze im Wasser, so ist dessen Leitfähigkeit gering und – ähnlich einem Vorwiderstand in einem elektrischen Stromkreis – die niedrige Wasserleitfähigkeit behindert die mögliche Sauerstoffkorrosion am Werkstoff deutlich. Die Bildung von Korrosionsprodukten wie z.B. Magnetit geht auf ein Minimum zurück. Übrigens bilden sich aus 1000l sauerstoffgesättigtem Füllwasser zunächst nur 36g Magnetit (ein Esslöffel Fe3O4). Echte Schlammprobleme haben also ihre Ursache im ständigen Zutritt von Sauerstoff, z.B. durch diffusionsoffene Fußbodenheizungsrohre, defekte Ausdehnungsgefäße oder auch häufiges Nachspeisen von Ergänzungswasser.
Die VDI 2035/2 begrenzt hier zu Recht für den sogenannten salzarmen Betrieb die Leitfähigkeit auf 100 µS/cm für das Umlaufwasser. Da die Leitfähigkeit ein Summenparameter für die im Wasser gelösten Salze ist, werden korrosionschemisch schädliche Stoffe wie Chlorid und Sulfat mit erfasst. Beim lochkorrosiven Chlorid beispielsweise gelten 30 bis 50 mg/l im Umlaufwasser als bedenklich (EN 14868, ÖNORM H5195), da die Wahrscheinlichkeit für Lochkorrosion im Heißwasser für bestimmte Edelstähle dann bereits merklich ansteigt.
Auch Nitrate im Umlaufwasser begünstigen – über eine chemische Reaktion zu Ammonium – die Spannungsriss-Korrosion an Messingteilen. Grundsätzlich gilt daher: Sind die Neutralsalze weitgehend aus dem Füllwasser entfernt, treten bestimmte Korrosionsarten erst gar nicht auf. Auch die mikrobiologische Aktivität ist regelrecht auf Diät gesetzt. Bei einer klassischen Enthärtung des Heizwassers wird dieser Vorteil aufgegeben.
Selbstalkalisierung kann für Aluminium gefährlich werden
Aluminium wird zunehmend in der Konstruktion von Wärmeerzeugern eingesetzt. Grund dafür ist unter anderem seine hervorragende Wärmeleitfähigkeit und die Möglichkeit, komplexe Formen durch Gusstechnik zu realisieren. Während andere Metalle eher hohe pH-Werte im Heizwasser zur Ausbildung einer schützenden Deckschicht benötigen, sind bei Aluminium pH-Werte über 8,5 schädlich. Die sogenannte Selbstalkalisierung des Heizungswassers tritt nennenswert nur bei enthärteten Wässern auf. Bei unbehandelten Trinkwässern ist sie minimal, bei VE-Wasser so gut wie nicht vorhanden.
Das übliche Enthärtungsverfahren führt im kalten Zustand noch zu keiner nennenswerten Veränderung des pH-Werts. Erst beim Erwärmen des Wassers wandelt sich das vorher im Enthärtungsprozess erzeugte Natriumhydrogenkarbonat (Natron) in Natriumkarbonat (Soda) um, eine Substanz, die man von Waschlaugen her kennt. Dabei werden in der Praxis pH-Werte bis 9,5 erreicht, die ein Bauteil innerhalb eines Jahres zerstören können. Diese Art der Heizwasseraufbereitung wird daher von den Kesselherstellern, die Aluminium einsetzen, untersagt. In der Praxis zeigt sich ein zu hoher pH-Wert für diesen Werkstoff in der Bildung von Wasserstoffgas. Im System, z.B. an Heizkörpern, wird häufiges Entlüften notwendig. Da für die Basenkorrosion des Aluminiums kein Sauerstoff notwendig ist, können auch korrosionstechnisch geschlossene Anlagen grundsätzlich davon betroffen sein.
Die umweltfreundlichste und sicherste Methode zum Schutz gegen Basenkorrosion ist auch hier der Einsatz von vollentsalztem Wasser, aus welchem die sodabildenden Ionen weitgehend entfernt sind. Hohe pH-Werte sind bei anderen Metallen jedoch durchaus erwünscht, da sich diese dann im Korrosionssystem passiv verhalten. Daher auch die Forderung in den Richtlinien VDI 2035, SWKI BT 102 und ÖNORM H5195-1 nach einem pH-Wert des Heizungswassers im Bereich von 8,2 bis 10,0.
Versauerung von Heizungswasser durch Sauerstoffkorrosion
Das Gegenteil der Selbstalkalisierung ist die Versauerung von Heizungswässern. Hauptprozess ist die Sauerstoffkorrosion, da so gut wie keine Anlage in der Praxis als korrosionstechnisch geschlossen gilt. Kommt Eisen mit Sauerstoff im wässrigen System zur Reaktion, wird Säure freigesetzt (für chemisch Interessierte: durch Hydrolyse des Eisen-III-Ions), die den pH-Wert leicht auf Werte um 6 absenkt. Bei diffusionsoffenen Anlagen wird gelegentlich sogar die Selbstalkalisierung enthärteter Wässer überkompensiert, daher zeigen oft auch Altanlagen, die nur enthärtet wurden, niedrige pH-Werte.
Passend hierzu, wenn es um die Frage des pH-Werts im Heizungswasser geht, ist auch die Aussage von Siemens Building Technologies in Bezug auf Regelventile (veröffentlicht im Österreichischen Installateur 7-8/2007): „Sämtliche Analysen von Problemanlagen der letzten zehn Jahre zeigen einen zu niedrigen pH-Wert.“ Ein anderes wasserchemisches Beispiel dafür ist die starke Versauerung von Seen in ehemaligen Braunkohletagebau-Gebieten durch die Oxidation von eisenhaltigem Grundwasser. Hier werden sogar pH-Werte kleiner 4 erreicht.
Kontraproduktiv in diesem Zusammenhang ist die weitverbreitete Behauptung, dass sich auch bei VE-Wasser der pH-Wert von selbst alkalisch einstellen soll. Tatsache ist, dass VE-Wasser keine Salze mehr enthält, die dieses bewerkstelligen können. Zunächst liefern die meisten Produkte zur Wasserbehandlung hier leicht saures Wasser, welches beim Ausgasen von Kohlensäure in den neutralen Bereich kommt, aber immer noch nicht – wie gefordert – alkalisch ist.
Die pH-Stabilisierung bleibt notwendige Maßnahme
Um den Schwankungen des pH-Werts vorzubeugen, muss das System etwas gepuffert werden, d.h., die Füllwasserzusammensetzung muss es ermöglichen, sowohl eine Alkalisierung des Wassers beim Erwärmen in der Anlage als auch eine Versauerung durch Korrosionsprozesse auszugleichen. Ein chemisch leeres Wasser kann dies nicht, es muss aber auch nur in eine Richtung, und zwar gegen Versauerung, stabilisiert werden.
Ein optimales Umlaufwasser ist salzarm und leicht alkalisch gepuffert. Enthärtete Wässer puffern zwar, alkalisieren aber meist zu stark für Aluminium und enthalten lochkorrosive Salze in unterschiedlicher Konzentration. Entsalzte Wässer wiederum sind kaum alkalisch und haben keine Pufferkapazität.
Als Ausweg aus diesem Dilemma kann das entsalzte Wasser entweder mit Rohwasser verschnitten werden oder es wird ein Puffersystem hinzugefügt. Wird mit Rohwasser gemischt, so müssen natürlich die Grenzwerte im Umlaufwasser für pH-Wert, Gesamthärte, Leitfähigkeit und beispielsweise Chlorid vom Installateur mit berücksichtigt werden. Einfacher und praxisgerechter sind hier Füllpatronen, die neben einer leicht alkalischen Harzmischung auch einen pH-Stabilisator mit einspülen, der auch für Aluminium im Heizsystem geeignet ist. Ein Beispiel ist hier die Permasoft-Serie von Perma-Trade Wassertechnik.
Praktische Maßnahmen gegen die Versauerung
Der pH-Wert im Umlaufwasser von Heizanlagen spielt eine tragende Rolle, da er darüber entscheidet, ob die darin enthaltenen Metalle zur Korrosion neigen. Von den Richtlinien her wird dafür ein alkalisches, von den meisten Herstellern aber auch salzarmes Wasser vorgegeben. Mischbettpatronen mit einem Überschuss an basischem Harz sind hierzu prinzipiell geeignet. Allerdings zeigt dieses nahezu mineralfreie Wasser keine Stabilität gegen pH-Wertverschiebungen nach unten, wie sie durch Sauerstoffkorrosion auftritt. Daher empfehlen sich zur Erstbefüllung Mischbettpatronen, die zusätzlich einen umweltfreundlichen, anorganischen pH-Stabilisator mit einspülen und die Leitfähigkeit trotzdem niedrig halten. Die jährliche Nachkontrolle, wie von der Richtlinie empfohlen, ist sinnvoll.
Info
pH-Wert (potentia Hydrogenii)
Der Säuregrad wird durch den dimensionslosen pH-Wert angegeben und ist ein Maß für die Konzentration an Wasserstoffionen (H+). Die Skala reicht im Wasser von 0 bis 14. Eine neutrale Flüssigkeit hat den Wert sieben, liegt der pH-Wert darüber, ist die Lösung basisch, darunter ist sie sauer. Da es sich um eine logarithmische Skala handelt, steigt die Säurekonzentration je ganzzahliger Stufe um Faktor zehn an. Das heißt, bei einem pH-Wert von 6,5 im Heizwasser ist der Säuregehalt hundertmal größer als bei einem pH-Wert von 8,5.
Autor
Dr. Dietmar Ende ist Entwicklungsleiter der Perma-Trade Wassertechnik GmbH in 71229 Leonberg, Telefon (0 71 52) 9 39 19-0, ende@perma-trade.de, https://www.perma-trade.de/